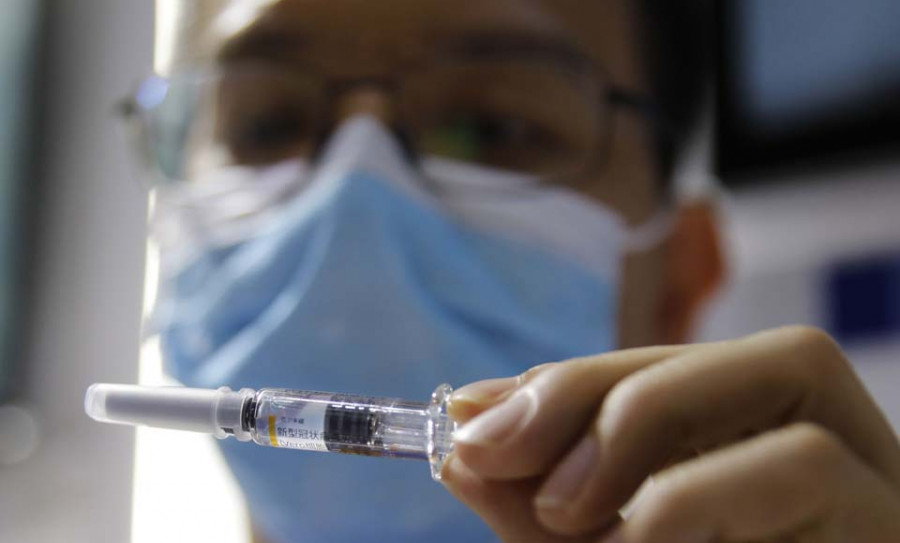
Los ensayos clínicos de la vacuna contra el coronavirus que están desarrollando la Universidad de Oxford y AstraZeneca, una de las mas prometedoras del mundo, se reanudarán tras ser interrumpidos por la reacción adversa sufrida por un voluntario.
Esta vacuna es una de varias que se están desarrollando en todo el mundo a gran velocidad a fin de contener la pandemia, que causó ya más de 28 millones de casos, más de 900.000 muertos y está castigando las economías.
En un comunicado, la universidad de Oxford indicó ayer que las pruebas clínicas de la sustancia, denominada ChAdOx1 nCoV-19 y desarrollada junto a la farmacéutica británica AstraZeneca, se reanudarán en el Reino Unido tras una pausa dispuesta el día 6 como medida de precaución.
Esta posible vacuna está en las fases finales de los ensayos clínicos antes de recibir la autorización de los organismos reguladores para proceder a inmunizar a la población.
A finales de agosto, la UE cerró con AstraZeneca un “primer contrato” que le garantizaba el acceso a 300 millones de dosis de la vacuna, por lo que la suspensión de los ensayos supuso un serio motivo de preocupación en Europa y en todo el mundo.
En su nota para dar cuenta de la reanudación de las pruebas, la universidad indicó que en todo el mundo unas 18.000 personas recibieron esta vacuna en estudio como parte de los ensayos clínicos y que, en pruebas tan amplias como esta, se espera que algún participante pueda sentirse mal.
“Cada caso debe ser evaluado cuidadosamente” para confirmar la seguridad de la vacuna, añadió el comunicado de Oxford, que no especificó la fecha de reanudación de los ensayos.
Las pruebas empezarán otra vez tras completarse la revisión independiente y tras el visto bueno de la Autoridad de Regulación de Medicinas para la Salud.
“No podemos desvelar la información médica sobre la enfermedad (del voluntario) por razones de confidencialidad del participante”, explicó la alta casa de estudio en su nota.
“Estamos comprometidos con la seguridad de nuestros participantes y el más alto nivel de conducta en nuestros estudios y seguiremos de cerca la seguridad” de las dosis, añaden.
Según los medios, las pruebas fueron interrumpidas después de que la universidad detectara una sospechosa inflamación de la médula espinal en una voluntaria del Reino Unido.
La potencial vacuna, que dio resultados prometedores en los primeros ensayos, estaba siendo sometida a pruebas clínicas en el Reino Unido, Estados Unidos, Brasil y Sudáfrica.
El mes pasado, los Gobiernos de Argentina y México, así como la fundación mexicana Slim, llegaron a un acuerdo con AstraZeneca y Oxford para fabricar la vacuna para sus países y distribuirla después al resto de América Latina, excepto Brasil.
El presidente de Argentina, Alberto Fernández, informó en agosto de que el objetivo era elaborar entre 150 y 250 millones de dosis que estarían disponibles a precios accesibles, con un coste individual de entre 3 y 4 dólares.
El contrato de la UE con la farmacéutica se rubricó en nombre de los Estados miembros y las dosis se distribuiría de forma proporcional en función de la población de cada país.
El proyecto de la vacuna está en las últimas fases después de que los resultados de los primeros ensayos, publicados el pasado julio, indicasen que era segura y “entrena” al sistema inmune contra el coronavirus.